Page 544 - Основы_химии
P. 544
538 Н. С. К У Р Н А К О В .
В связи с этим теплота растворения быстро охлажденных и закаленных
сплавов сильно разнится от соответствующей величины для механических
смесей. Последняя величина при растворении смеси грамм-молекул NaCI и
KCl в 100 грамм-молекулах воды = 5700 кал.; для закаленных ниже 0° спла
вов того же состава теплоты растворения найдены равными от — 3620 кал.
(Оствальд, 1882) до — 3607 кал. (Курнаков и Жемчужный, 1906). Таким
образом при указанных условиях образование двойной грамм-молекулы
твердого раствора поглощает от —2080 до —2093 кал. При сохранении
сплавов названная разница между теплотами растворения медленно умень
шается; только после нагревания в течение нескольких дней при 85 —150°
она становится равной нулю, и распадающаяся система приближается
к состоянию механической смеси чистых NaCI и KCl. Природными про
дуктами такого распадения являются кристаллы минерала хлоронатрока-
лита, встречающегося в вулканических возгонах [Лакруа, 1906; Джон-
стон-Левис, 1908; Миеле, 1910). Аналогические распадения непрерывных
твердых растворов свойственны также сплавами NaCl-LiCi (Жемчужный
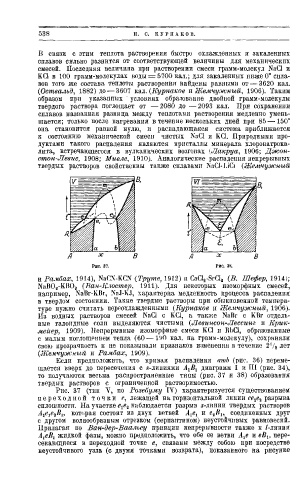
Л х В Л
Рис. 37. Рис. 38.
и Рамбах, 1914), NaCN-KCN (Труте, 1912) и CaCl 2-SrCl ä (В. Шефер, 1914);
NaBCyKBOj (Ван-Клостер, 1911). Для некоторых изоморфных смесей,
например, NaBr-Kßr, NaJ-KJ, характерна медленность процесса распадения
в твердом состоянии. Такие твердые растворы при обыкновенной темпера
туре нужно считать переохлажденными (Курнаков и Жемчужный, 1906).
Из водных растворов смесей NaCI с KCl, а также Na'ßr с КВг отдель
ные галоидные соли выделяются чистыми (Левинсон-Лессинг и Крик-
мейер, 1909). Непрерывные изоморфные смеси KCl и RbCl, образованные
с малым поглощением тепла ( 6 0 — 1 У 0 кал. на грамм-молекулу), сохраняли
свою прозрачность п не показывали признаков изменения в течение 2Ѵа лет
(Жемчужный и Рамбах, 1909).
Если предположить, что кривая распадения nmb (рис. 36) переме
щается вверх до пересечения с А-лиииями А ХВ Х диаграмм I и III (рис. 34),
то получаются весьма распространенные типы (рис. 37 и 38) образования
твердых растворов с ограниченной растворимостью.
Рис. 37 (тип V, по Розебуму IV) характеризуется существованием
п е р е х о д н о й ' т о ч к и е, лежащей на горизонтальной линии ее уе^ разрыва
сплошности. На участке e te t наблюдается разрыв s-линии твердых растворов
А^^^Н,, которая состоит из двух ветвей A te t и eji^ соединенных друг
с другом волнообразным отрезком (серпантином) неустойчивых равновесий.
Прилагая по Ван-дер-Ваальсу принцип непрерывности также к /-линии
жидкой фазы, можно предположить, что обе ее ветви А хе пере
А$В Х и еВ ѵ
секающиеся в переходной точке е, связаны между собою при посредстве
неустойчивого узла (с двумя точками возврата), показанного на рисунке